○ 루게릭병(Lou Gehrig's disease) = 근위축성측삭경화증(Amyotrophic lateral sclerosis, ALS)
○ ALS의 시작(onset), 진행(progression) 그리고 예후(prognosis) 등에 대한 역치를 결정하는 요인으로는 개인의 유전적 요인, 노화요인 그리고 환경요인 등으로 제시되지만 가족 중 2명 이상의 ALS 환자가 있는 가족형(familial) ALS (fALS)와 단지 1명만 환자가 있는 산발형(sporadic) ALS(sALS) 모두에서 공통적으로 유전 결함이 확인되고 있다. 지금까지 ALS와 관련하여 25-30 유전자가 확인되지 있지만 유전적 변이(genetic variation)에 대한 개인별 감수성의 차이에 따라 ALS 발병에 차이가 있는 것도 사실이다(Family Caregiver Support, 2022). 따라서 치료제 개발은 환자집단의 유전-역학적 특징을 우선적으로 확인할 필요성이 있다.
1. 몰타(Malta)의 ALS 환자의 유전자 분석
① 몰타에서의 연구: 질환의 유전학적 특징을 이해하기 위해서는 지리적으로 고립되고 특정 질환의 환자가 존재하여야 한다. 이러한 측면에서 Borg 등(2021)에 의해 Fig. 1에서 처럼 몰타 섬에서 수행된 ALS 환자에 대한 유전자 분석은 ALS와 유전적 특징을 확인하는 좋은 연구라고 할 수 있다. 몰타의 ALS 유병률(prevalence rate)은 단위인구 100,000명 당 3.44명이다.
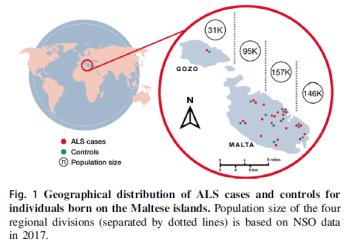
② 환자-대조군: 몰타의 전체인구는 약 5십만명으로 이중 2017년에서 2018년 사이 환자 24명 그리고 대조군 13명과 더불어 case-control 연구를 통해 유전자 분석이 이루어졌다.
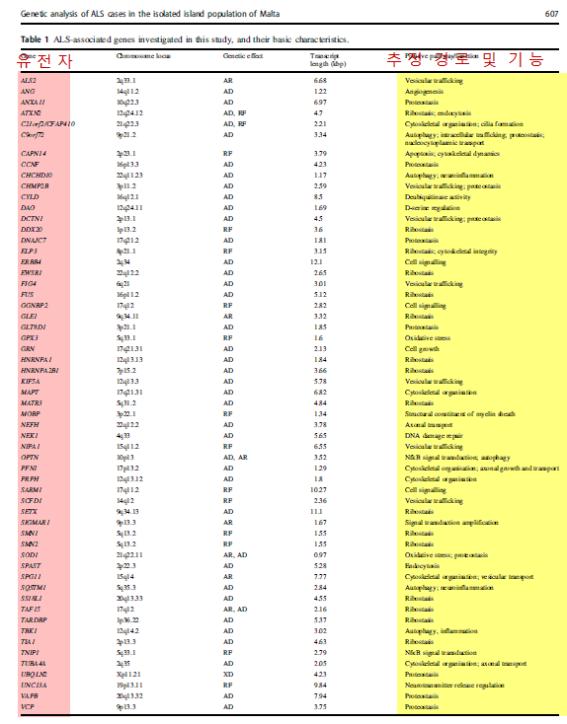
③ ALS-관련 유전자: Table 1에서처럼 대조군과 비교하여 58개의 유전자가 ALS와 관련이 있는 것으로 환자-대조군 연구로부터 조사되었다.
2. 몰타 ALS 환자의 특징
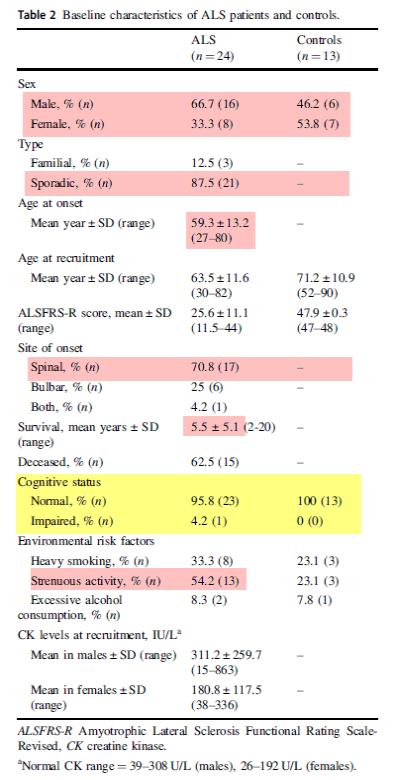
① ALS 환자의 남녀 비율: Table 2는 ALS 환자와 대조군의 특성을 나타낸 것이다. ALS 환자 중 남자가 66.7%, 반면에 여자는 33.3로 남자가 약 2배 정도 많은 것으로 조사되었다.
② fALS vs sALS: 가족형인 fALS는 12.5%, 반면에 산발형인 sALS는 87.5% 등으로 조사되었으며 산발형 ALS가 높다는 것은 대부분의 연구 결과와 유사한 결과 이다.
③ 연령: ALS 발병의 평균 연령은 59.3 ± 13.2세이며 발병 연령의 분포는 27세에서 80세까지이다. 발병의 정점 연령은 남성에서 50-59세 사이, 여성인 경우에는 70에서 79세 사이로 확인되었다. Male-to-female incidence ratio(발병비율) 1.98로 남자가 2배 정도 ALS 발병률이 높았다.

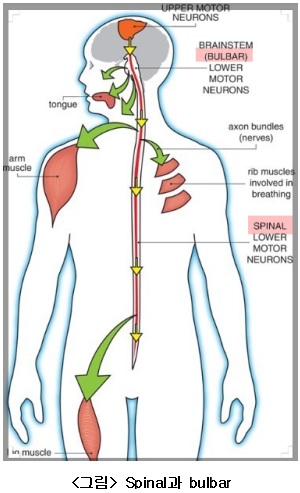
④ 발병 시작부위: <그림>에서처럼 척수(spinal)에서 70.8%, 뇌의 하부운동신경(lower motor neurons)에 영향을 주는 연수(bulbar, 뇌간의 하부)에서 25% 그리고 척추와 연수에서 동시 발명이 4.2%로 확인되었다.
⑤ 발병 후 생존 기간: 평균 생존기간은 5.5 ± 5.1년으로 추정되었다.
⑥ 환경 요인: 환자-대조군의 ALS 원인에 대한 환경 요인로는 흡연, 강도 높은 육체적 활동 그리고 지나친 음주 3개로 분류하여 분석한 결과, 강도 높은 육체적 활동에서 환자 및 대조군이 각각 54.2%와 23.1%로 가장 크게 차이가 확인되었다.
⑦ 인지기능: ALS-관련 유전자의 돌연변이 및 결함이 단순히 ALS의 병리기전뿐만 아니라 전두측두엽 치매(Frontotemporal dementia, FTD), 파킨슨병(Parkinson's disease; 기타 신경퇴행성질환) 등과 동반하여 발생한다는 것이 확인되고 있다. 이와 관련하여 대조군에서는 발생하지 않았지만 몰타의 ALS 환자에서는 약 4.2%에서 인지장애가 확인되었다. 그러나 이 정도의 비율로의 인지장애가 ALS와 연관하여 공통 유전자적 요인으로 인과성을 확인하기는 다소 무리이다.
3. 몰타 ALS 환자의 유전자 특징
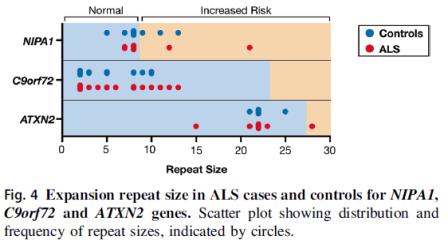
○ 유럽인의 대부분 ALS 환자에게서 C9orf72와 더불어 SOD1, TARDBP 그리고 FUS 등의 유전자에서 돌연변이가 나타난다. 그러나 Fig.4에서처럼 몰타의 fALS 및 sALS 환자에서는 C9orf72의 염기서열의 expansion repeated size가 증가하였지만 ALS risk 증가에서는 문제점이 없는 것으로 확인되었다. 반면에 몰타의 fALS 및 sALS 환자에서는 NIPA1과 ATXN2 유전자의 expansion repeated size 증가 그리고 ALS risk가 증가하는 것이 확인되었다. 그 외 ALS2, DAO, DCTN1, ERBB4, SETX, SCFD1 그리고 SPG11 등에서 ALS-관련 변이체가 확인되었다. 즉, 전체 sALS 환자의 40%에서 ALS-관련 유전자에서 변이성이 확인되었지만 fALS 환자의 2/3에서는 ALS-관련 유전자와는 연관성이 없었다.
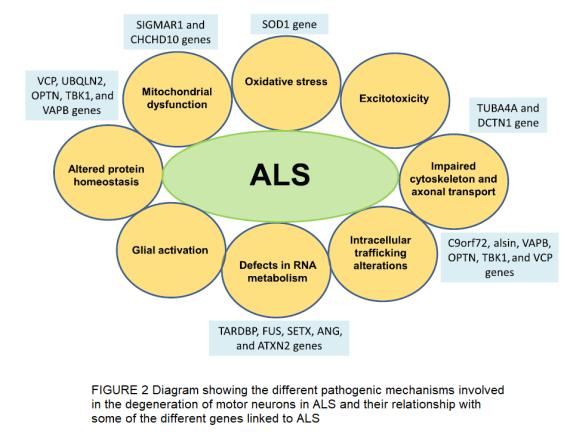
4. 몰타(Malta)의 ALS 환자의 유전자 분석에서 결론: 몰타는 섬으로 이루어진 작은 국가로 비교적 타 지역과 분리되어 몰타 지역의 특징적 ALS 환자의 유전자 변이체 확인이 가능하다고 할 수 있다. 결과적으로 몰타 지역의 ALS 환자의 50%가 잘 알려진 ALS-관련 유전자 돌연변이와는 관련이 없는 것으로 확인되었다. 따라서 ALS 발병은 잘 알려진-유전자 변이와 상관없이 발병할 수 있으며 특히 지역적으로 고립되면 이런 현상은 더 확연하다고 할 수 있다. 이와 같은 결론은 일반적으로 ALS와 관련된 병리기전, 즉 다음과 같은 8가지 MOA(mechanism of action)가 FIGURE 2에서처럼 유전자적 연관성이 어떻게 이루어지는가에 대한 연구가 필요하다고 할 수 있다.
① G lutamate excitotoxicity와 같은 흥분세포독성(excitotoxicity)
② 신경아세포 활성화(glial activation) 및 자가면역성기전에 의한 만성 염증
③ 유해활성산소종 또는 산화적 스트레스( oxidative stress)
④ 신경세포간 물질이동의 이상에 의한 신경영양물질 등의 결핍
⑤ 운동신경세포의 골격( cytoskeleton) 및 축삭(axon)의 운반에서 이상
⑥ RNA metabolism의 결함
⑦ 단백질 항산성의 변화
⑧ 미토콘드리아의 기능저하
5. ALS의 유전자적 진단과 전체 유전체 염기서열 분석
○ ALS의 유전적 진단은 환자의 예후를 비롯하여 때론 유전자-표적 치료 및 관리에 정보까지 제공할 수 있다. 그러나 앞서 예시처럼 지역별 또는 환자별 유전자의 결함 유무는 너무 다양하여 ALS 진단에는 다소 한계가 있다고 할 수 있다. 특히 ALS의 조기 진단은 예방뿐만 아니라 질병의 초기부터 관리에 도움이 될 수 있다. 이러한 측면에서 ALS 유전자적 진단의 표준화(standard diagnostic genetic test for ALS) 필요성이 제시되고 있으며 전체 유전체 염기서열 분석(whole-genome sequencing, WGS) 또는 전장유전체분석이 대안으로 제시되고 있다.
1) Grassano 등(2022)의 논문
○ Grassano 등(2022)은 ALS의 진단 표준화를 위해 전체 유전체의 염기서열 분석방법인 전장 유전체 시퀀싱(Whole genome sequencing, WGS)을 환자-대조군 코호트 연구를 제시하였다.
○ 이탈리아의 피에몬테(Piemonte)와 발레 다오스타(Valle D'Aosta)에 거주하는 1043 ALS 환자와 대조군 755명 건강한 성인을 대상으로 42의 ALS-관련 유전자의 변이체와 C9orf72와 ATXN2의 반복-염기서열 확장(repeated-expansions) 등에 대해 WGS를 수행하였다.
2) fALS vs sALS의 유전자 돌연변이 분포
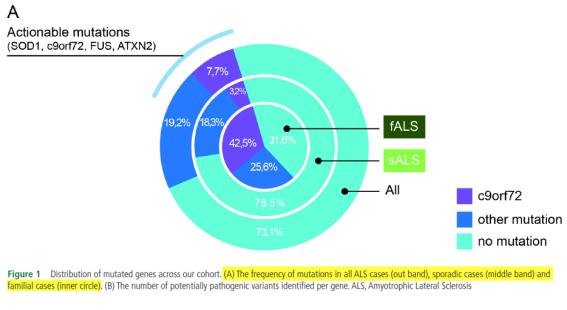
○ fALS 환자군에서는 C9orf72 유전자 돌연변이가 42.5%, 다른 유전자 돌연변이가 25.6% 그리고 돌연변이가 확인되지 비율이 31.6%로 조사되었다(Figure 1의 A). sALS 환자군에서 C9orf72 유전자 돌연변이가 3.2%, 다른 유전자 돌연변이가 18.3% 그리고 돌연변이가 확인되지 비율이 78.5%로 조사되었다. fALS 환자군와 sALS 환자군의 통합으로 각각 7.7%, 19.2% 그리고 73.1%로 조사되었다. 이는 fALS 환자군에서는 유전자 돌연변이에 의한 인과성 높고 반면에 sALS는 인과성이 낮지만 전반적으로 유전자 요인 및 유전자 외적 요인에 의한 ALS 발병률이 3:7의 ratio로 추정할 수 있다.
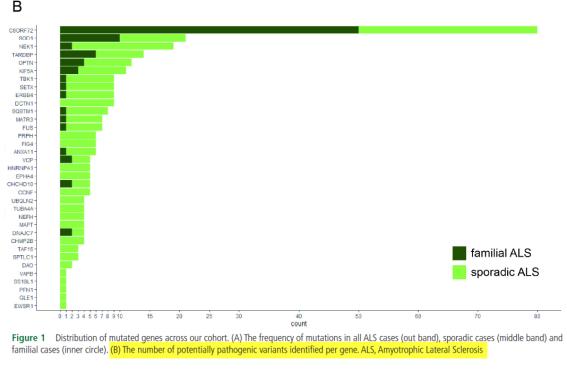
○ Figure 1의 B)는 1043 ALS 환자 중 fALS와 sALS 환자군에서 확인된 돌연변이 유전자별 분포를 나타낸 것이다. 연구 결과에 따르면 203명의 ALS 환자로부터 96 유전자로부터 돌연변이가 확인되어 전체 환자 중 19.5%에서 돌연변이가 확인되었다. 가장 많이 돌연변이가 발생한 유전자는 전체 ALS 환자군에서 C9orf72 유전자로 7.7%, 그리고 SOD1 유전자에서 2.0%, NEK1 유전자에서 1.8%, TARDBP 유전자에서 1.4% 그리고 KIF5A 유전자에서 0.8%가 확인되었다.
3) 조기 발현(early-onset)과 지연 발현(late-onset)에서 돌연변이 관점
○ fALS 환자군 88명에서 약 75.2%가 유전자 돌연변이가 확인되었다. 이들 중 연령 기준으로 50세 미만의 조기 발현 환자들은 43.9%, 그리고 75세 이상의 지연 발현 환자들은 19.7%로 분포하였다. 특히 지연 발현 환자군과 비교하여 조기 발현 환자들에서 유전자 돌연변이율이 훨씬 높았다.
4) 반복-염기서열 확장(repeated-expansions)
○ 반복-염기서열 확장 분석에서 ALS 발현과 가장 높은 위험성을 가진 유전자의 반복서열은 Intermediate-length ATXN2 CAG expansion (30 -33 repeats)으로 추정 되었으며 교차비(odds ratio)가 2.0 이상이었다.
5) 다유전자 돌연변이의 빈도
○ ALS 환자 중 다유전자(oligogenic) 돌연변이 환자는 1.3%, 단일 유전자(monogenic) 돌연변이 가진 환자는 25.6%, 그리고 돌연변이를 가지지 않은 환자(non-mutated cases)에서는 73.1%로 확인되었다.
6) 결론
○ 대부분 연구에서처럼 본 연구에서도 sALS 환자군 중 fALS에서 sALS보다 더 높은 유전자 돌연변이가 확인되어 유전체 염기서열 분석(whole-genome sequencing, WGS)에 의한 ALS 진단은 다른 방법보다 큰 차이가 없을 것으로 된다. 그러나 엑솜 시퀀싱(Whole exome sequencing, WES) 및 타겟 패널 시퀀싱(Targeted panel sequencing, TPS)과 비교하여 광범위한 영역이 분석된다. 이는 상대적으로 각 영역별 시퀀싱 깊이(depth)는 낮아지기 때문에 분석정확도가 낮아질 수 있다. 반면에 인트론과 비번역 부위(untranslated region)을 분석할 수 있기 때문에 구조적(structural) 변이나 유전자 발현 조절과 관련된(regulatory) 변이를 검출할 수 있는 장점도 있다. 끝으로 예상은 되었지만 본 연구에서 지연 발현 환자군과 비교하여 조기 발현 환자들에서 유전자 돌연변이율이 훨씬 높았다는 점은 참고할만하다.
6. 루게릭병과 유전-역학적 연구에 대한 결론
○ 인구 집단에서 ALS 발현의 유전-역학적 특징은 일부 유전자에서 높은 빈도의 돌이변이율은 있지만 지역적 및 집단적 특성에 따라 차이가 있을 수 있다. 이와 같은 인간집단에서 역학적 특성에 대한 이해는 항루게릭 약물 개발에 있어서 대단히 중요한 점이라고 할 수 있다. 오늘날 루게릭병의 치료제로 개발된 3가지 약물인 iluzole, edaravone, 그리고 masitinib 등이 동물시험에서는 safety와 efficacy가 확인되었지만 실제 환자들에게 치료제로의 실패는 특정-유전자 및 특정-병리기전 기반으로 개발되었기 때문이다. 즉, 인간집단의 유전-역학적 특성을 고려하지 않은 동물모델에 대한 의존성이 높았다는 것이다. 특히 저분자 합성의약품은 동물과 사람의 종간 차이가 너무 크다는 것은 약물 개발에서 항상 인식하여야 할 점이다.
